Cómo encontrar el estado de oxidación y carga iónica de un elemento
Escrito por Sean Lancaster ; última actualización: February 01, 2018
El estado de oxidación de un elemento juega un rol crítico en su reactividad y estabilidad. Describe el número de electrones intercambiados con otros elementos durante una reacción química. Los estados de oxidación le ayudan a un químico a decidir si una reacción dada es del tipo oxidación-reducción, como una deposición electroquímica, o una de las otras clases de reacciones posibles. Los iones poliatómicos liberados en soluciones interactúan con el solvente y, por lo general, con otros iones o elementos. Debes calcular la carga de cada elemento en el ión en base a la carga de sus otros elementos. Debes poder determinar el estado de oxidación de cualquier elemento y la carga asociada con él.
Examina la tabla periódica. Puedes ver fácilmente que los elementos neutrales tienen un número electrones igual a su número atómico. La carga en el átomo es cero y el estado de oxidación también.
Encuentra las cargas iónicas posibles para cada elemento, usando la tabla periódica. La regla del octeto indicará cuántos electrones requiere cada elemento para llegar a una configuración estable de ocho electrones.
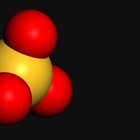
Equilibra los iones poliatómicos para lograr la carga correcta. Cada elemento tendrá potencialmente una carga distinta. El estado de oxidación del elemento es igual a su carga. Por ejemplo, encuentra el estado de oxidación y carga iónica de los elementos en SO4^2- y MnO4^1. El oxígeno necesita dos electrones para completar su octeto. El estado de oxidación del O es (-II). La carga en el oxígeno es -2. Usar esto para calcular la carga en S y Mn lleva a SO4^-2. La carga del ión es -2 y la expresión x + 4 * (-2) = -2, por lo tanto, x = +6 y la carga de Mn es y + 4 * (-2) = -1, lo que equivale a +7.
Calcula el estado de oxidación del elemento, que equivale a su carga. Siguiendo el ejemplo, S^+6 tiene un estado de oxidación de S(VI) y Mn^+7 de Mn(VII).
Más artículos
Cómo calcular el número de moléculas→

¿Cómo encontrar el número de iones en un elemento?→
Cómo obtener el número total de valencias en un compuesto →

Propiedades de valencia variable→

¿Cómo puedo convertir las fórmulas químicas en nombres de compuestos?→
Cómo saber si una ecuación es una reacción redox→
